Emicolectomia destra totalmente laparoscopica per il trattamento dei tumori del colon ascendente
Dr. Francesco Roscio, Dr. Ildo Scandroglio
Divisione di Chirurgia Generale – Presidio Ospedaliero “Galmarini”, Tradate Dipartimento di Chirurgia – Azienda Ospedaliera “Ospedale di Circolo”, Busto Arsizio
Il tumore colorettale (CRC) rappresenta nel mondo la terza neoplasia più frequente nel sesso maschile e la seconda in quello femminile, con un’incidenza assoluta che è aumentata dai 945.000 nuovi casi/anno del 2000 a 1.234.000 nuovi casi/ anno nel 2008[I] [II]. Le stime di sopravvivenza a 5-anni per CRC variano dal 54,0% nei alcuni paesi europei inclusi nello studio Eurocare-4 al 63,5% di alcune regioni nordamericane afferenti al network epidemiologico Surveillance Epidemiology and End Results (SEER-17)[III]. I tumori del colon destro rappresentano approssimativamente il 15% di tutti i CRC, con un picco di incidenza nella settima decade di età. Negli ultimi venti anni, i progressi tecnologici e la standardizzazione delle tecniche chirurgiche hanno contribuito ad una progressiva diffusione della chirurgia laparoscopica colorettale (LCS). I vantaggi a breve termine di LCS rispetto alle colectomie open sono ben noti, ed includono minor dolore, ridotto impegno respiratorio, una precoce canalizzazione ed una degenza postoperatoria più breve con ritorno più rapido alla vita attiva da parte del paziente[IV] [V] [VI].Questi vantaggi sembrano derivare da un minore stress chirurgico provocato da LCS, e quindi da una ridotta risposta sistemica in seguito a chirurgia laparoscopica[VII]. Inoltre, recenti trials clinici randomizzati (RCTs) e metanalisi hanno dimostrato, con livello di evidenza 1, risultati oncologici quantomeno sovrapponibili tra chirurgia mininvasiva del colon ed approccio tradizionale superando definitivamente alcune passate criticità in merito a metastasi su port-sites o a scarsa adeguatezza oncologica delle resezioni laparoscopiche[I] [II] [III] [IV]. Per inciso, anche riguardo alla chirurgia laparoscopica del retto, l’analisi preliminare degli esiti a lungo termine sembra mostrare risultati incoraggianti, sebbene i maggiori RCTs siano tuttora in corso[v].
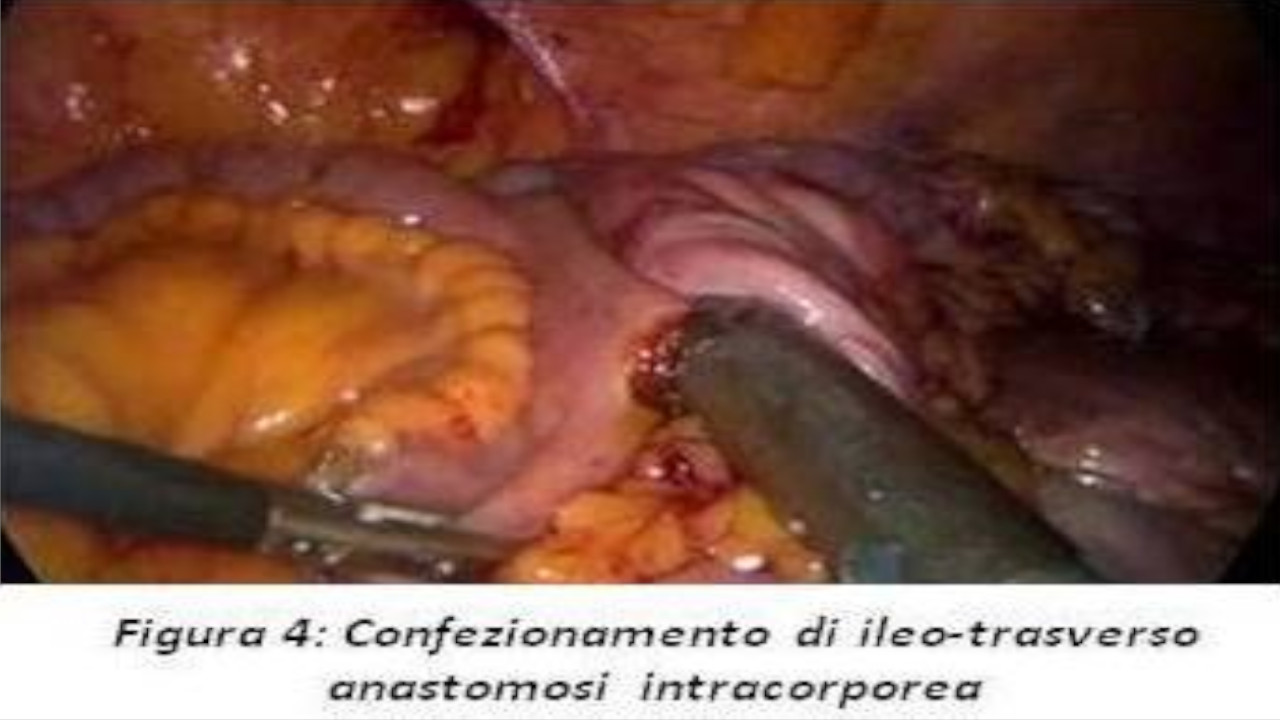
Curiosamente, 8 delle 20 procedure laparoscopiche oggetto del primo report circa LCS da parte di Jacobs et coll. nel 1991, erano emicolectomie destre laparo-assistite[VI]. Nonostante questa iniziale dimostrazione di riproducibilità tecnica però, la colectomia destra laparoscopica non ha registrato negli anni una diffusione comparabile a quella di altre procedure mininvasive colorettali. Segnalazioni riguardo a questa tecnica risultano infatti meno frequenti rispetto a casistiche pubblicate sull’emicolectomia sinistra o le resezioni di retto per via laparoscopica. Il trattamento mininvasivo dei tumori del colon destro è di norma rappresentato da una emicolectomia destra laparo-assistita (LARC), con confezionamento di anastomosi ileo-colica extracorporea (ECA). Nel recente passato, alcune esperienze hanno comparato i risultati dell’emicolectomia destra open con quelli della LARC, senza evidenza di differenze statisticamente significative in termini di morbidità e sopravvivenza tra i due gruppi[VI] [VII] [IX]. L’emicolectomia destra totalmente laparoscopica (TLRC), con anastomosi intracorporea (ICA), rappresenta invece una tecnica considerata più impegnativa, e come tale proposta da un esiguo numero di Autori[X] [XI]. Entrambe le varianti tecniche, LARC e TLRC, riconoscono un approccio da mediale a laterale. Tuttavia LARC prevede che il tempo vascolare e la mobilizzazione viscerale siano eseguiti per via laparoscopica, mentre i momenti resettivo ed anastomotico-ricostruttivo siano extracorporei. In TLRC invece, tutti i tempi operatori sono puramente intracorporei, ed in tal senso questa viene considerata una tecnica totalmente laparoscopica. Una recente inchiesta ad opera di Jamali et coll. ha intervistato 35 chirurghi laparoscopisti di grande esperienza in merito al grado di difficoltà e fattibilità delle varie procedure laparoscopiche colorettali, al fine di individuare un corretto percorso formativo in tale ambito. Dall’analisi delle risposte, gli Autori hanno concluso che l’emicolectomia destra laparoscopica è tecnicamente più impegnativa della sigmoidectomia[xii]. Inoltre, il livello di difficoltà aumenta significativamente da LARC a TLRC, giustificando il perché molti chirurghi scelgano di eseguire una emicolectomia destra per via laparoscopica con confezionamento extracorporeo dell’anastomosi.Diversi studi hanno analizzato il tema della curva di apprendimento in LCS, la quale, secondo la letteratura, può essere considerata completata dopo un numero molto variabile di procedure, addirittura compreso tra le 30 e le 70 a seconda dei diversi Autori[XIII] [XIV] [XV].
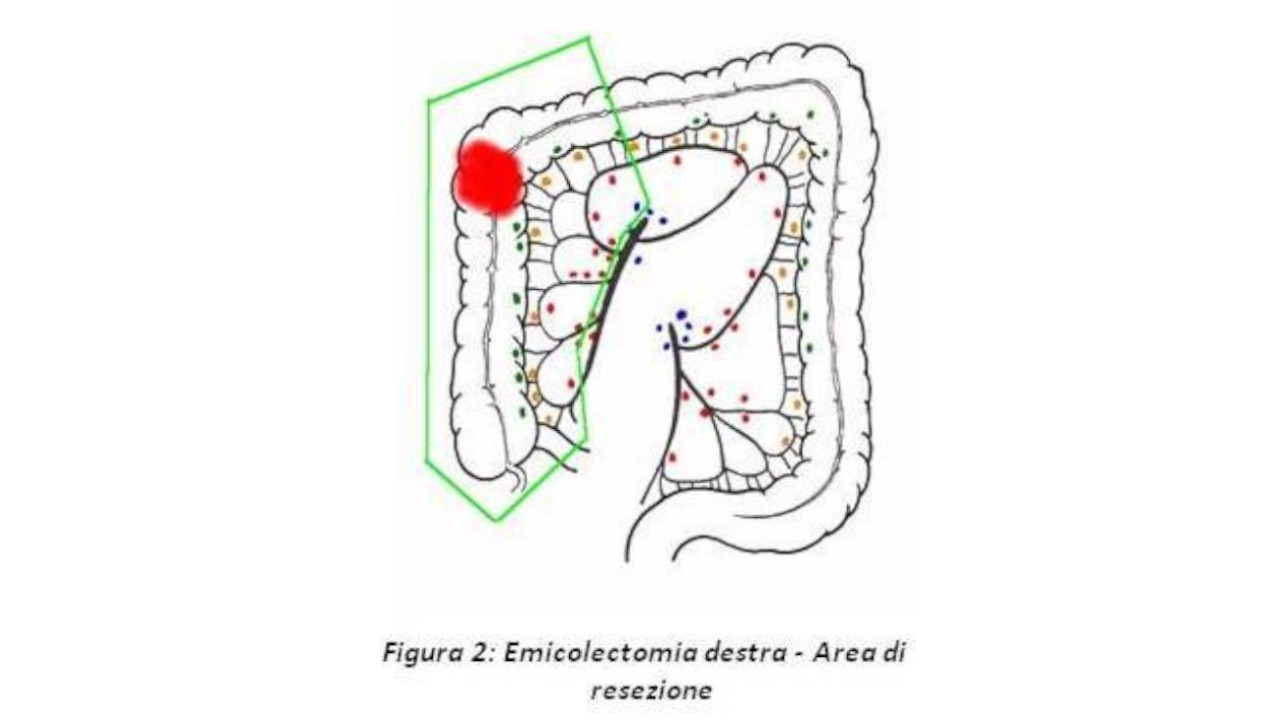
Risultati così numericamente difformi sono da attribuire al fatto che una curva di apprendimento riflette una molteplicità di fattori, dalla selezione dei pazienti alla disponibilità di risorse e tecnologie. E’ inoltre importante sottolineare come in questo campo il raggiungimento di una proficiency, ovvero di una adeguatezza nell’eseguire un determinato intervento, debba significare non solo l’ottenimento di una fattibilità tecnica, ma soprattutto quello di una correttezza oncologica. Nello specifico, non abbiamo sicuri dati riguardo alla learning curve dell’emicolectomia destra laparoscopica, se non per Tekkis et al., i quali quantificano in 55 e 62 casi le curve di apprendimento rispettivamente per l’emicolectomia laparoscopica destra e sinistra[xvi]. Come detto, il punto nodale è rappresentato dal raggiungimento di un livello appropriato di adeguatezza oncologica. Gli attuali standards di radicalità in chirurgia colorettale includono la legatura prossimale del tronco arterioso tributario, adeguati margini di resezione liberi da malattia, una reale “no-touch isolation technique” che eviti ogni manipolazione o perforazione del tumore, l’estrazione protetta del reperto anatomico ed una appropriata dissezione linfonodale con almeno 17 linfonodi asportati[xvii] [xviii] [xix]. In tal senso, noi riteniamo che una corretta linfoadenectomia sia diretta conseguenza di adeguate legature vascolari, che devono necessariamente essere eseguite in sede intracorporea, attraverso clips laparoscopiche od Endostaplers, tanto in LARC quanto in TLRC. Dunque, una legatura extracorporea del tronco ileo-ceco-colico attraverso la minilaparotomia, così come inizialmente suggerito da Young-Fadok et al., ha dimostrato di essere non solo più impegnativa, ma soprattutto oncologicamente meno sicura, e come tale dovrebbe essere abbandonata[xx]. L’isolamento e la sezione prossimale dei vasi ileo-ceco-colici consente inoltre di eseguire la dissezione linfonodale lungo l’asse della vena mesenterica superiore (SMV)in senso caudo-craniale fino al tronco di Henle.
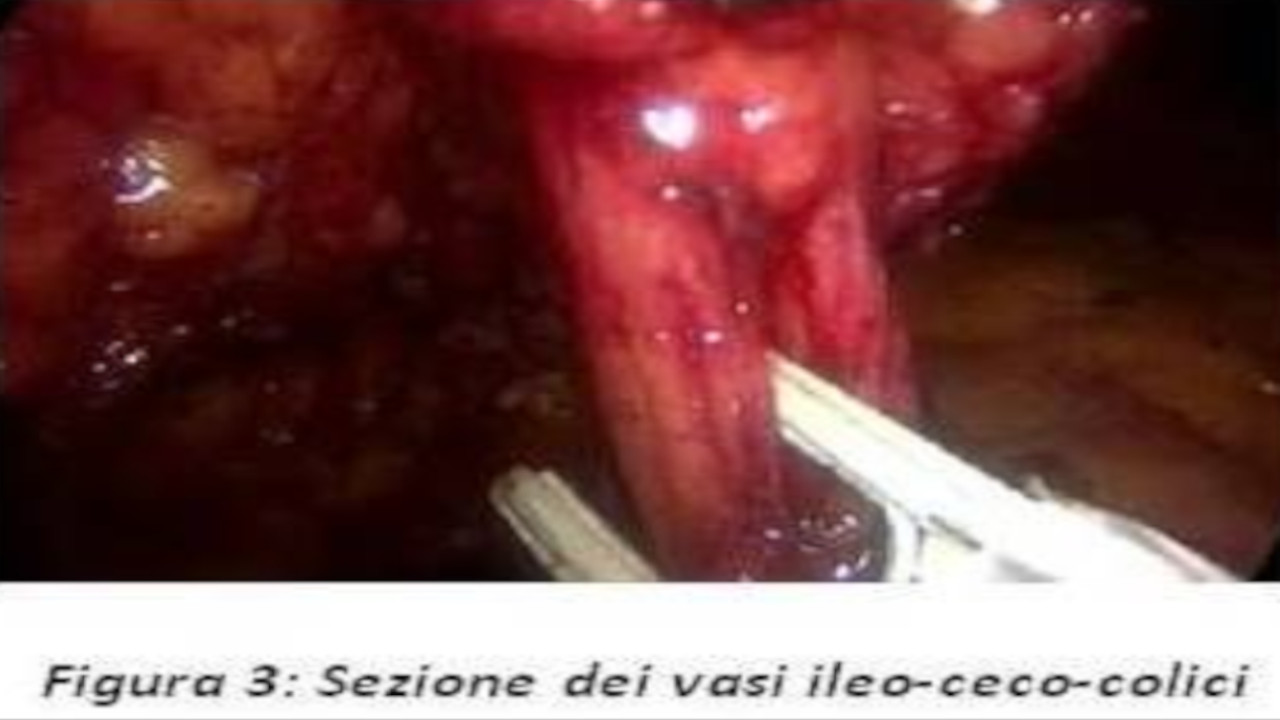
E’ bene ricordare come l’anatomia vascolare del colon destro sia spesso variabile. Alcuni studi anatomici post-mortem hanno evidenziato come in oltre il 50% dei pazienti possano mancare arteria e vena colica destra, la quale, se presente, di solito drena nel tronco gastrocolico[I][II]. Il razionale oncologico che sottende alla scheletrizzazione linfonodale sistematica della SMV è suggerito da un 3,1% di metastasi riportate a questo livello su 14.144 pazienti osservati dalla Japanese Society for Cancer of the Colon and Rectum[iii]. Inoltre, nella nostra esperienza, un’adeguata linfoadenectomia a livello del tronco di Henle – linfonodi gastro-epiploici di destra – è da raccomandarsi in caso di neoplasia della flessura epatica o del traverso prossimale, nonché in tutti i casi di tumore di stadio II o superiori. Come per tutta LCS, anche nell’emicolectomia destra laparoscopica l’approccio di scelta è medio-laterale[iv]. Nonostante questa tecnica possa apparire meno familiare ad alcuni chirurghi, in quanto ribalta diametralmente il classico approccio latero-mediale delle procedure open, essa consente, unitamente al controllo vascolare precoce, l’identificazione immediata del piano di cellulare lasso tra fascia di Toldt e di Gerota, il quale con l’ausilio del pneumoperitoneo viene dissecato, consentendo una corretta separazione tra mesocolon e retroperiotoneo, nonché minimizzando il rischio di lesioni verso le strutture retroperitoneali. Tale approccio consente così di ottenere una sicurezza oncologica attraverso una reale “no touch isolation technique”[v]. Nella attuale letteratura sono presenti alcuni lavori che comparano gli outcomes a breve termine di LARC e TLRC, senza evidenziare differenze statisticamente significative circa i tempi operatori o i tassi di conversione, ma con alcuni vantaggi in termini di ridotta morbi-mortalità e degenza post-operatoria a favore della tecnica totalmente laparoscopica[vi] [VII] [VIII] [IX]. Nella nostra esperienza, i pazienti operati mediante TLRC registrano un timing di canalizzazione statisticamente inferiore rispetto a LARC, e questo dato si riflette proporzionalmente sui risultati di degenza post-operatoria[x]. Tecnicamente, al fine di minimizzare il rischio di una stenosi anastomotica, suggeriamo che ICA venga eseguita attraverso il confezionamento di una anastomosi latero-laterale meccanica con carica adeguata, seguita dalla chiusura della breccia enterotomica residua mediante sutura manuale in duplice strato a partenza dall’apice inferiore. LARC mostra poi un tasso di conversione e di complicanze maggiore nei soggetti obesi rispetto ai non-obesi[XI], benchè in mani esperte tale confronto non raggiunga livelli di significatività statistica[XII]. Raftopolous et al. hanno ottenuto risultati sostanzialmente sovrapponibili dopo TLRC in pazienti obesi e non obesi, confermando la sicurezza e l’efficacia di questa tecnica per coorti di pazienti con body mass index superiore a 40 m2/kg[xiii]. Nella ferma convinzione che, in generale, i pazienti obesi possano beneficiare di LCS rispetto alle procedure convenzionali, crediamo che TLRC rappresenti il trattamento ideale per questa tipologia di pazienti in quanto evita l’estrazione di un colon destro non ancora deafferentato attraverso una parete addominale di spessore superiore alla media. Inoltre, l’esteriorizzazione di mesi corti e pesanti richiede minilaparotomie di lunghezza superiore, ed aumenta il rischio di microlacerazioni che potrebbero danneggiare il buon esito della successiva anastomosi. Riteniamo che una ICA ileo-colica presenti alcuni vantaggi rispetto ad una corrispettiva ECA. Il confezionamento intracorporeo dell’anastomosi, infatti, consente una costante visione dell’intero campo operatorio. Questo favorisce il corretto orientamento dei monconi anastomotici, minimizzando il potenziale “twisting” dell’ileo sul proprio asse. TLRC permette una appropriata sintesi della breccia mesenteriale sotto visione laparoscopica, che noi raccomandiamo di eseguire sempre, a punti staccati o con l’utilizzo di colla di fibrina, onde escludere il pericolo di ernie interne post-operatorie. Inoltre, come già accennato, ICA evita eccessive trazioni dei visceri e dei tessuti attigui alla minilaparotomia, riducendo il rischio ischemico per i monconi anastomotici e la parete addominale. Ulteriori vantaggi segnalati di TLRC includono una minore formazione di aderenze dovuta all’assenza di manipolazione intestinale ed un potenziale decremento del rischio di trombosi venosa mesenterica. Infine, il confezionamento di ICA consente di rimuovere il colon asportato attraverso qualsivoglia sede di incisione addominale, mentre in LARC la sede della minilaparotomia è vincolata dalla situazione anatomica del colon destro. La lunghezza dell’incisione cutanea rappresenta un altro argomento di discussione, sebbene a nostro avviso di importanza secondaria, e nelle diverse casistiche risulta statisticamente inferiore nei pazienti sottoposti a TLRC. Tecnicamente, la minilaparotomia che segue la creazione di ICA ha infatti esclusivamente lo scopo di estrarre un tratto anatomico già resecato, mentre in LARC l’incisione cutanea dovrebbe essere sufficientemente generosa da permettere l’esteriorizzazione del colon destro e dell’ultima ansa ileale, la loro sezione ed una successiva ECA, evitando accuratamente, come detto, la compressione dei mesi. L’incidenza di laparoceli dopo procedure laparoscopiche colorettali si attesta intorno all’8%, con una presentazione più frequente sulle incisioni mediane rispetto alle paramediane[xiv]. Sembra che incisioni site al quadrante superiore destro possano impattare negativamente sulla performance respiratoria dei pazienti, con conseguente ipossia tissutale e quindi aumentato rischio di infezione di ferita ed ernie incisionali[xv]. In tal senso, il nostro attuale orientamento è verso una minilaparotomia trasversa sovrapubica.
Nella nostra esperienza, dunque, TLRC rappresenta una tecnica fattibile e sicura, che risulta in un incoraggiante outcome a breve termine, una bassa incidenza di complicanze maggiori ed il rispetto dei principi di radicalità oncologica, senza pesare sui tempi operatori.
Bibliografia
[1] Colorectal cancer incidence and mortality worldwide in, http://globocan.iarc.fr/factsheets/cancers/colorectal 2008.
[1] Parkin DM, Bray F, Ferlay J, Pisani P. Estimating the world cancer burden: Globocan 2000. Int J Cancer 2001; 94: 153-6.
[1] Airtum Working Group. Report 2011. Epidemiol Prev 2011; 35(Suppl. 3): 33-4.
[1] Schwenk W, Haase O, Neudecker J, Muller JM. Short-term benefits for laparoscopic resection. Cochrane Database Syst Rev 2005; 20(3): CD003125.
[1] Weeks JC, Nelson H, Gelber S, Sargent D, Schroeder G, Clinical Outcomes of Surgical Therapy (COST) Study Group. Short-term quality-of-life outcomes following laparoscopic-assisted colectomy vs. open colectomy for colon cancer: a randomized trial. J Am Med Assoc 2002; 287: 321-8.
[1] Veldkamp R, Kuhry E, Hop WC, Jeekel J, Kazemier G, Bonjer HJ, et al, Colon cancer Laparoscopic or Open Resection Study Group (COLOR). Laparoscopic surgery versus open surgery for colon cancer: short-term outcomes of a randomised trial. Lancet Oncol 2005; 6: 477-84.
[1] Wu FPK, Sietses C, von Blomberg BME, van Leeuwen PAM, Meijer S, Cuesta MA. Systemic and peritoneal inflammatory response after laparoscopic or conventional colon resection in cancer patients: a prospective, randomized
trial. DisColonRectum 2003; 46: 147-55.
[1]ColonCancer Laparoscopic or Open Resection Study Group. Buunen M, Veldkamp R, Hop WC, Kuhry E, Jeekel J, Haglind E, et al. Survival after laparoscopic surgery versus open surgery for colon cancer: long-term outcome of a randomised clinical trial. Lancet Oncol 2009; 10: 44-52.
[1] Lacy AM, Delgado S, Castells A, Prins HA, Arroyo V, Ibarzabal A, et al. The longterm results of a randomized clinical trial of laparoscopy-assisted versus open surgery for colon cancer. Ann Surg 2008; 248: 1-7.
[1] Kuhry E, Schwenk W, Gaupset R, Romild U, Bonjer HJ. Long-term results of laparoscopic colorectal cancer resection. Cochrane Database Syst Rev 2008; 16(2): CD003432.
[1] Jayne DG, Thorpe HC, Copeland J, Quirke P, Brown JM, Guillou PJ. Five-year follow-up of the Medical Research Council CLASSIC trial of laparoscopically assisted versus open surgery for colorectal cancer. Br J Surg 2010; 97: 1638-45.
[1] Van der Pas MH, Haglind E, Cuesta MA, Fürst A, Lacy AM, Hop WC, Bonjer HJ; COlorectal cancer Laparoscopic or Open Resection II (COLOR II) Study Group. Laparoscopic versus open surgery for rectal cancer (COLOR II): short-term outcomes of a randomised, phase 3 trial. Lancet Oncol 2013 Mar; 14(3): 210-8. doi: 10.1016/S1470 2045(13)70016-0.
[1] Jacobs M, Verdeja JC, Goldstein HS. Minimally invasive colon resection (laparoscopic colectomy). Surg Laparosc Endosc 1991; 1: 144-50.
[1] Zheng MH, Feng B, Lu AG, Li JW, Wang ML, Mao ZH, et al. Laparoscopic versus right hemicolectomy with curative intent for colon carcinoma. World J Gastroenterol 2005; 11: 323-6.
[1] Hamel CT, Pikarsky AJ, Weiss E, Nogueras J, Wexner SD. Do prior abdominal operations alter the outcome of laparoscopically assisted right hemicolectomy? Surg Endosc 2000; 14: 853-7.
[1] Baker RP, TituLV, Hartley JE, Lee PW, Monson JR. A case-control study of laparoscopic right hemicolectomy versus open right hemicolectomy. DisColonRectum 2004; 47: 1675-9.
[1] Bergamaschi R, Schochet E, Haughn C, Burke M, Reed III JF, Arnaud JP. Standardized laparoscopic intracorporeal right colectomy for cancer: short-term outcome in 111 unselected patients. Dis Colon Rectum 2008; 51: 1350-5.
[1] Casciola L, Ceccarelli G, Di Zitti L, Valeri R, Bellochi R, Bartoli A, et al. Laparoscopic right hemicolectomy with intracorporeal anastomosis. Technical aspects and personal experience. Minerva Chir 2003; 58: 621-7.
[1] Jamali FR, Soweid AM, Dimassi H, Bailey C, Leroy J, Marescaux J. Evaluating the degree of difficulty of laparoscopic colorectal surgery. Arch Surg 2008; 143: 762-7.
[1] Schlachta CM, Mamazza J, Seshandri PA, Cadeddu M, Gregoire R, Poulin EC. Defining a learning curve for laparoscopic colorectal resections. DisColonRectum 2001; 44: 217-22.
[1] Bennett CL, Stryker SJ, Ferriera MR, Adams J, Beart Jr RW. The learning curve for laparoscopic colorectal surgery: preliminary results from a prospective analysis of 1194 laparoscopic-assisted colectomies. Arch Surg 1997; 132: 41-4.
[1] Dincler S, Koller MT, Steurer J, Bachmann LM, Christen D, Buchmann P. Multidimensional analysis of learning curves in laparoscopic sigmoid resection: eight-year results. DisColonRectum 2003; 46: 1371-8.
[1] Tekkis PP, Senagore AJ, Delaney CP, Fazio VW. Evaluation of the learning curve in laparoscopic colorectal surgery: comparison of right-sided and left-sided resections. Ann Surg 2005; 242: 83-91.
[1] Nelson H, Petrelli N, Carlin A, Couture J, Fleshman J, Guillem J, et al. Guidelines 2000 for colon and rectal cancer surgery. J Natl Cancer Inst 2000; 93: 583-96.
[1] Guidelines for laparoscopic resection of curable colon and rectal cancer. SAGES Publication #32, http://sages.org/publications.html July 2005.
[1]GoldsteinNS,SanfordW, Coffey M, Layfield LJ. Lymph node recovery from colorectal resection specimens removed for adenocarcinoma. Trends over time and a recommendation for a minimum number of lymph nodes to be recovered. Am J Clin Pathol 1996; 106: 209-16.
[1] Young-Fadok TM, Nelson H. Laparoscopic right colectomy: five-step procedure. DisColonRectum 2000; 43: 67-71.
[1] Yamaguchi S, Kuroyanagi H, Milsom JW, Sim R, Shimada H. Venous anatomy of right colon: precise structure of major veins and gastrocolic trunk in 58 cadavers. DisColonRectum 2002; 45: 1337-40.
[1] Jin G, Tuo H, Sugiyama M, Oki A, Abe N, Mori T, et al. Anatomic study of the superior right colic vein: its relevance to pancreatic and colonic surgery. Am J Surg 2006; 191: 100-3.
[1] Yamaguchi S. Laparoscopic right hemicolectomy with intracorporeal anastomosis. Tech Coloproctol 2010; 14: 365-6.
[1] Veldkamp R, Gholghesaei M, Bonjer HJ, Meijer DW, Buunen M, Jeekel J, Anderberg B, Cuesta MA, Cuschierl A, Fingerhut A, Fleshman JW, Guillou PJ, Haglind E, Himpens J, Jacobi CA, Jakimowicz JJ, Koeckerling F, Lacy AM, Lezoche E, Monson JR, Morino M, Neugebauer E, Wexner SD, Whelan RL. Laparoscopic resection of colon cancer: consensus of the European Association of Endoscopic Surgery (EAES). Surg Endosc 2004; 18: 1163-85.
[1] Pigazzi A, Hellan M,Ewing DR, Paz BI, Ballantyne GH. Laparoscopic medial-tolateral colon dissection: how and why. J Gastrointest Surg 2007; 11: 778-82.
[1] Hellan M, Anderson C, Pigazzi A. Extracorporeal versus intracorporeal anastomosis for laparoscopic right hemicolectomy. JSLS 2009; 13: 312-7.
[1] Scatizzi M, Kröning KC, Borrelli A, Andan G, Lenzi E, Feroci F. Extracorporeal versus intracorporeal anastomosis after laparoscopic right colectomy for cancer: a case-control study. World J Surg 2010; 34: 2902-8.
[1] Fabozzi M, Allieta R, Brachet Contul R, Grivon M, Millo P, Lale-Murix E, et al. Comparison of short- and medium-term results between laparoscopically assisted and totally laparoscopic right hemicolectomy: a case-control study. Surg Endosc 2010; 24: 2085- 91.
[1] Chaves JA, Idoate CP, Fons JB, Oliver MB, Rodríguez NP, Delgado AB, et al. A case-control study of extracorporeal versus intracorporeal anastomosis in patients subjected to right laparoscopic hemicolectomy. Cir Esp 2011; 89: 24-30.
[1] Roscio F, Bertoglio C, De Luca A, Frattini P, Scandroglio I. Totally laparoscopic versus laparoscopic assisted right colectomy for cancer. Int J Surg 2012; 10: 290-5.
[1] Pikarsky AJ, Saida Y, Yamaguchi T,MartinezS, Chen W, Weiss EG, et al. Is obesity a high-risk factor for laparoscopic colorectal surgery? Surg Endosc 2002; 16: 855-8.
[1] Dostalík J, Martínek L, Vávra P, Andel P, Gunka I, Gunková P. Laparoscopic colorectal surgery in obese patients. Obes Surg 2005; 15: 1328-31.
[1] Raftopoulos I, Courcoulas AP, Blumberg D. Should completely intracorporeal anastomosis be considered in obese patients who undergo laparoscopic colectomy for benign or malignant disease of the colon? Surgery 2006; 40: 675-82.
[1] Singh R, Omiccioli A, Hegge S, McKinley C. Does the extraction-site location in laparoscopic colorectal surgery have an impact on incisional hernia rates? Surg Endosc 2008; 22: 2596-600.
[1] Nakamura T, Mitomi H, Ihara A, Onorato W, Sato T, Ozawa H, et al. Risk factors for wound infection after surgery for colorectal cancer. World J Surg 2008; 32: 1138-41.




